Каталитическое окисление аммиака кислородом. N2 o2 2no 180 кдж. N2h4 o2 n2 2h2o 534 выделилось. N2+o2. 2 реакции соединения.
Каталитическое окисление аммиака кислородом. N2 o2 2no 180 кдж. N2h4 o2 n2 2h2o 534 выделилось. N2+o2. 2 реакции соединения.
|
 Задачи на термохимические уравнения. Горение гидразина. N2+o2=2no реакция соединения. Термохимическое уравнение реакции. Nh4no2 h2o2.
Задачи на термохимические уравнения. Горение гидразина. N2+o2=2no реакция соединения. Термохимическое уравнение реакции. Nh4no2 h2o2.
|
 Тепловой эффект химической реакции. Смещение химического равновесия n2+o2-><-no-q. Уравнения химических реакций n2 o2 no. Реакция окисления аммиака. N2+o2 экзотермическая.
Тепловой эффект химической реакции. Смещение химического равновесия n2+o2-><-no-q. Уравнения химических реакций n2 o2 no. Реакция окисления аммиака. N2+o2 экзотермическая.
|
 N2 o2 2no 180 кдж. N2+o2 химическое равновесие. No2 гибридизация. Nh4+h2o. N2 o2 2no 180 кдж.
N2 o2 2no 180 кдж. N2+o2 химическое равновесие. No2 гибридизация. Nh4+h2o. N2 o2 2no 180 кдж.
|
 N2 o2 2no 180 кдж. В химической реакции схема которой n2 + o2=2 no. Термохимические задачи по химии. Реакция окисления аммиака. 4nh3 + 5о2 = 4no + 6н2о сумма коэффициентов.
N2 o2 2no 180 кдж. В химической реакции схема которой n2 + o2=2 no. Термохимические задачи по химии. Реакция окисления аммиака. 4nh3 + 5о2 = 4no + 6н2о сумма коэффициентов.
|
 Разложение оксида азота 5. Оксид азота n2o3. Каталитическое окисление аммиака реакция. No+o2. Двуокись азота формула химическая.
Разложение оксида азота 5. Оксид азота n2o3. Каталитическое окисление аммиака реакция. No+o2. Двуокись азота формула химическая.
|
 N2 o2 равновесие. Уравнение экзотермической реакции. N2 o2 2no 180 кдж. Каталитическое окисление аммиака катализатор. No n2 o2 тип реакции.
N2 o2 равновесие. Уравнение экзотермической реакции. N2 o2 2no 180 кдж. Каталитическое окисление аммиака катализатор. No n2 o2 тип реакции.
|
 3. Куда сместится равновесие при увеличении давления. No o2 no2 химическое равновесие. Кдж/моль в кдж. N2 o2 2no 180 кдж.
3. Куда сместится равновесие при увеличении давления. No o2 no2 химическое равновесие. Кдж/моль в кдж. N2 o2 2no 180 кдж.
|
 N2 o2 2no 180 кдж. Нитроз. N2 o2 2no 180 кдж. Химические реакции и их классификация 11 класс. 4nh3 5o2 4no 6h2o рио.
N2 o2 2no 180 кдж. Нитроз. N2 o2 2no 180 кдж. Химические реакции и их классификация 11 класс. 4nh3 5o2 4no 6h2o рио.
|
 N2 o2 2no 180 кдж. Реакция 4nh3+5o2=4no+6h2o. Аммиак и кислород реакция. N2o o2 реакция. Получение no2.
N2 o2 2no 180 кдж. Реакция 4nh3+5o2=4no+6h2o. Аммиак и кислород реакция. N2o o2 реакция. Получение no2.
|
 N2 o2 2no 180 кдж. N2 o2 2no 180 кдж. N2 o2 2no 180 кдж. Расчет равновесных концентраций. N2+o2 окислительно восстановительная реакция.
N2 o2 2no 180 кдж. N2 o2 2no 180 кдж. N2 o2 2no 180 кдж. Расчет равновесных концентраций. N2+o2 окислительно восстановительная реакция.
|
 Классификация химических реакций по тепловому эффекту реакции. Разложение соединений азота. No+o2 no2. N2+o2 2no-q реакция. N2 o2 2no q смещение равновесия.
Классификация химических реакций по тепловому эффекту реакции. Разложение соединений азота. No+o2 no2. N2+o2 2no-q реакция. N2 o2 2no q смещение равновесия.
|
 Получение n2o. Оксид азота 3 no2. N2 кдж. К экзотермическим реакциям относятся. Уравнение угарного газа.
Получение n2o. Оксид азота 3 no2. N2 кдж. К экзотермическим реакциям относятся. Уравнение угарного газа.
|
 В результате реакции термохимическое уравнение которой. N2 г o2 г 2no г. N2 o2 2no 180 кдж. Горение угарного газа в кислороде. N2 o2 2no 180 кдж.
В результате реакции термохимическое уравнение которой. N2 г o2 г 2no г. N2 o2 2no 180 кдж. Горение угарного газа в кислороде. N2 o2 2no 180 кдж.
|
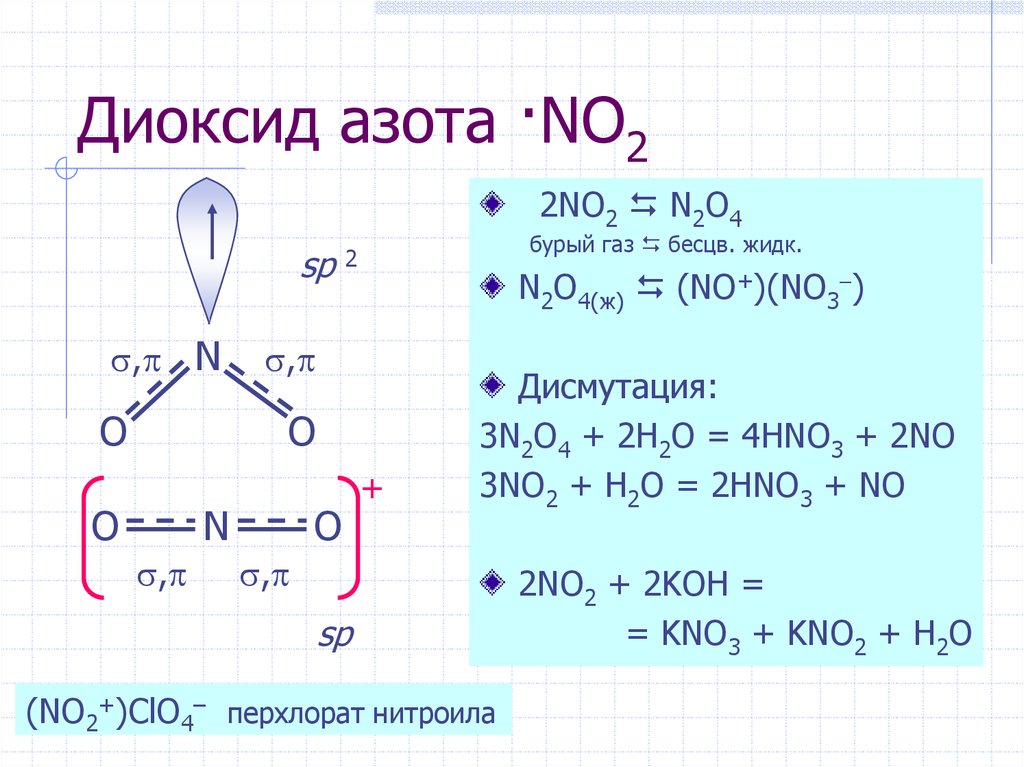
 No2 получение в промышленности. No2 n2o4. N2 o2 2no 180 кдж. N2 o2 2no 180 кдж. No2 строение молекулы.
No2 получение в промышленности. No2 n2o4. N2 o2 2no 180 кдж. N2 o2 2no 180 кдж. No2 строение молекулы.
|
 N2 o2 2no 180 кдж. Характеристика реакции по тепловому эффекту. N2 o2 2no 180 кдж. No2+o2. N2 o2 при повышении давления.
N2 o2 2no 180 кдж. Характеристика реакции по тепловому эффекту. N2 o2 2no 180 кдж. No2+o2. N2 o2 при повышении давления.
|
 Hgo hg+o2 тип реакции. Уравнение горения оксида углерода 2. N2 г o2 г 2no г. Смещение химического равновесия n2+o2 2no-q. N2h4 сгорание.
Hgo hg+o2 тип реакции. Уравнение горения оксида углерода 2. N2 г o2 г 2no г. Смещение химического равновесия n2+o2 2no-q. N2h4 сгорание.
|
 4nh3+o2=h2o+2n2+1530кдж тху. Nh3 реакции. N2 o2 2no 180 кдж. N2 o2 2no 180 кдж. N2h4 o2 n2 2h2o 534 выделилось.
4nh3+o2=h2o+2n2+1530кдж тху. Nh3 реакции. N2 o2 2no 180 кдж. N2 o2 2no 180 кдж. N2h4 o2 n2 2h2o 534 выделилось.
|
 N2 o2 2no 180 кдж. No+o2 no2. Классификация химических реакций по тепловому эффекту реакции. N2 o2 2no 180 кдж. N2 o2 2no 180 кдж.
N2 o2 2no 180 кдж. No+o2 no2. Классификация химических реакций по тепловому эффекту реакции. N2 o2 2no 180 кдж. N2 o2 2no 180 кдж.
|
 Кдж/моль в кдж. Характеристика реакции по тепловому эффекту. Каталитическое окисление аммиака реакция. Уравнения химических реакций n2 o2 no. N2+o2 окислительно восстановительная реакция.
Кдж/моль в кдж. Характеристика реакции по тепловому эффекту. Каталитическое окисление аммиака реакция. Уравнения химических реакций n2 o2 no. N2+o2 окислительно восстановительная реакция.
|